彭承宏医生的科普号
- 精选 胰腺肿瘤,开腹,腹腔镜,机器人,到底该如何选择?
很多患者生了胰腺肿瘤,对于手术方式的选择可以说到了纠结的地步,因为获得的信息往往不对称,什么意思,就是和你交流的医生,也许在沟通的时候存在一定的倾向性,比如这个医生不会做微创,他本身反对微创,可能会极
金佳斌 副主任医师 上海瑞金医院 普外科8295人已读 - 精选 胰腺术后出院注意事项
胰腺手术有其特殊性,出院后的恢复更需要医患双方的共同努力,以下是一些注意事项:少量多餐,每三餐之间加1到2餐,睡前加一餐,少油饮食,流质1到3个月,期间建议增加蛋白粉(流质的形式)补充。慢慢过渡到半流
 金佳斌 副主任医师 上海瑞金医院 普外科2.1万人已读
金佳斌 副主任医师 上海瑞金医院 普外科2.1万人已读 - 精选 彭承宏专家就诊流程
部分患者看病难,一部分也是难在对流程的不解,以为见到医生就什么都解决了,医生看病更多的是依赖有限的病历资料。为方便就诊,特制作门诊咨询流程,免去繁琐沟通。
彭承宏 主任医师 上海瑞金医院 普外科7953人已读 - 精选 胰腺良性与交界性肿瘤的机器人手术
摘要近年来, 随着医学影像学技术的发展, 良性及交界性胰腺肿瘤如黏液性囊性肿瘤(MCN)、实性假乳头状肿瘤(SPN)、导管内乳头状黏液性肿瘤(IPMN)、神经内分泌肿瘤(pNET)等的发现率也随之提高
彭承宏 主任医师 上海瑞金医院 普外科8310人已读 - 精选 国外科学顶级期刊在线发表瑞金医院胰腺微创手术重大研究成果
https://web.shobserver.com/news/detail?id=220344目前,胰腺癌的手术主要有开腹手术、腹腔镜微创手术、机器人微创手术等。外科“机器人”时代已然来临,但无论是学界还是大众都存在疑惑:胰腺癌预后差,机器人手术究竟有必要吗?开腹胰十二指肠切除术涉及多个器官组织的切除与吻合,机器人能胜任吗?为了解答这一问题,3月4日,国外科学顶级期刊《美国医学会杂志外科学》(JAMA Surgery)在线发表了上海交通大学医学院附属瑞金医院胰腺中心沈柏用、彭承宏教授团队机器人胰腺手术的最新研究成果。文章总结了近10年来瑞金医院胰腺中心完成的机器人胰腺微创手术,重点分析了胰十二指肠切除术这一最高难度的普外科手术。除此之外,国际顶尖外科学杂志《Annals of Surgery》《Surgery》《Surgical Endoscopy》等近半年连续发表了瑞金医院胰腺中心的临床研究和临床总结的文章。目前,瑞金医院胰腺中心每年收治胰腺癌患者超过2500例,机器人手术例数在全球排名第二,注重在确保规范的基础上不断创新治疗方法,并对每位患者在基因检测的基础上采用个体化精准综合治疗方案。目前,该中心也是全国唯一可使用医保报销进行胰腺癌术后基因检测的机构。
彭承宏 主任医师 上海瑞金医院 普外科4736人已读 - 精选 机器人胰腺手术各类术式进展及介绍
我们来谈谈机器人胰腺手术,胰腺外科进入微创时代,机器人手术则是科技转化到医学的经典案例。胰腺手术本身代表着复杂、凶险、辛苦,机器人技术则是精密、稳重、放松,故操作机器人做胰腺手术,可以说把优势放大,把劣势缩小,从而带来更优质的医疗。 机器人辅助腔镜手术系统最早于1999年应用于心脏外科。进入21世纪以来,由于传统腹腔镜技术存在种种不足之处,机器人外科手术系统逐渐受到外科医师的重视。与腹腔镜手术相比,机器人手术系统采用了三维而不是二维的高清立体视觉,恢复了手眼协调,且滤除了术者自身不能控制的自然颤动。对胰腺手术来说,其不仅降低术者的疲劳程度,更因其具备7个自由度的机械臂可在胰腺所处的腹膜后微小空间内操作使解剖、切除及缝合更加简便。2003年,Melvin等[1]报道第一例机器人胰体尾切除术。同年,Giulianotti等[2]报道13例机器人胰腺手术,包括8例胰十二指肠切除术和5例胰体尾切除术。2010年,国内周宁新等[3]最早报道了机器人胰腺手术,此后,越来越多的机器人胰腺手术被报道,术式涵盖开腹的各类胰腺手术。规则性胰腺切除术规则性胰腺切除包括胰十二指肠切除、胰体尾切除和全胰切除。胰十二指肠切除术由于其手术部位位于后腹膜、手术局部区域血管关系复杂以及需行3个吻合,以重建消化道等原因被认为是腹部手术中最具挑战性和最复杂的手术之一。所以,自Gagner等[4]第一次报道腹腔镜胰十二指肠切除术以来,该术式始终难以广泛展开。Giulianotti等[2]于2003年第一次报道8例机器人胰十二指肠切除术(5例Whipple术和3例Traverso-Longmire术),平均手术时间为490 min,并发症和手术病死率分别为37.5%和12.5%。根据Giulianotti等[5]的经验,胰十二指肠切除术的一个重要的步骤便是解剖和离断胰腺钩突,利用助手和机器人系统的第三操作臂的配合可有效减少这一步骤的出血。相比之下,对于开放手术来说,为给胰腺和静脉之间留出足够空间,牵拉胰腺时空肠的小分支出血的风险很高,有时甚至会引起静脉撕裂。2010年,周宁新等[3]首次在国内报道8例机器人胰十二指肠切除术,并与8例开腹胰十二指肠切除术进行比较,发现前者的手术时间、术中出血量、出院时间及并发症发生率均优于后者。目前为止尚无比较腹腔镜和机器人胰十二指肠切除术的前瞻性随机临床试验,有关大宗机器人胰十二指肠切除术病例的研究仍为数不多,仅4篇文献比较机器人与开放胰十二指肠切除术[6-9]。这些文献指出,机器人手术组的术后并发症发生率在0~75%,包括0~35%的术后胰漏;病死率在0~4.5%,与开放手术组相似。根据Zhang等的荟萃分析[10],相较于开腹手术组,机器人手术组的并发症发病率下降12%。2016年,Liao等[11]报道的荟萃分析纳入了780例腹腔镜胰十二指肠切除术及248例机器人胰十二指肠切除术,发现两者的术后胰漏发生率无显著差异。刘荣等[12]提出,LR式机器人胰十二指肠切除术,认为其简化流程,提高手术效率。总体来讲,各家的手术流程基本与开放或腔镜的流程大同小异,熟练的配合、固定的流程可明显缩短手术时间,成熟的机器人胰十二指肠切除术应控制在总时间4~6 h。在肿瘤学方面,Chalikonda等[7]第一次对机器人和传统方法行胰十二指肠切除术作了病例对照研究,该研究共纳入60例病人,机器人手术组的R0切除率是100%,而开放手术组的R0切除率仅87%。2012年,Zeh等[13]报道了50例行机器人胰十二指肠切除术的壶腹部肿瘤病人,R0切除率为89%,中位淋巴结清扫数为18枚。然而,其他一些团队的经验报道所提及的淋巴结清扫数量并未达到指南的标准[7, 8, 14]。诚然,不同中心之间的数据由于术者经验和医疗系统不同,难以标准化比较。此外,外科医师往往会选择给肿瘤恶性程度更高的病人或肥胖的病人行开腹手术,数据中存在一定偏倚,所以一些结果倾向于微创技术比开腹手术更具优势。由于不需消化道重建,胰体尾切除术是微创技术应用最广的胰腺切除术。Melvin等[1]报道第一例机器人胰体尾联合脾切除术,用于治疗胰腺神经内分泌肿瘤,病人于术后第2天出院。同年,Giulianotti等[2]报道5例机器人胰体尾切除术,其中3例为胰腺癌,行联合脾切除术,平均手术时间为270 min,并发症和手术病死率分别为20%和0。2006年至2010年期间,Kang等[15]对45例病人行微创保脾胰体尾切除术,通过比较25例腹腔镜手术和20例机器人手术发现机器人组的保脾率显著升高(失败/成功, 9/16 比 1/19,P=0.027)。匹兹堡大学医学中心对其于2004年至2011年期间所行的所有微创胰体尾切除术进行回顾性分析,比较30例机器人胰体尾切除术及94例腹腔镜胰体尾切除术的围术期情况、90 d内并发症发生率及死亡率,结果发现尽管机器人组的病理恶性率更高,其中转开腹率仍显著低于腹腔镜组,且其余安全性指标均无明显差异,认为机器人胰体尾切除术是优于腹腔镜胰体尾切除术的[16]。然而,2015年,Butturini等[17]报道一项纳入43例病人的前瞻性非随机单中心研究,认为机器人及腹腔镜系统各有优劣,胰漏发生率相当,难以以一种标准化的方式比较两者。此外,在肿瘤学方面,大量研究报道机器人胰体尾切除术的根治效果优于腹腔镜胰体尾切除术。机器人组的肿瘤切缘阳性率一般为0[16-19],而腹腔镜组的肿瘤切缘阳性率在0~26%[20-22]。机器人组的淋巴结清扫数为5~19枚[5, 16-19],而腹腔镜组的淋巴结清扫数一般为6~-14枚[22-25]。机器人下的全胰切除报道较少,早期经验证明其可行性,且可降低住院时间。Giulianotti等[26]于2007年至2010年间完成5例机器人全胰切除术,平均手术时间456 min,平均估计术中出血量310 mL,无一例中转开腹或死亡。Zeh等[27]在2008年至2012年间完成5例机器人全胰切除术,其中1例中转开腹。平均手术时间503 min,平均估计术中出血量1 000 mL,高于该中心其他机器人手术。Boggi等[28]完成11例机器人全胰切除,发现与行传统全胰切除术相比,行机器人全胰切除术需更长手术时间,但相对估计术中出血量更少,且其余评估恢复情况的指标均比行传统手术的病人更具优势。我院也完成11例机器人全胰切除,由于机器人的左右移动性,可在不变换体位不增加trocar布局的情况下,实现全胰解剖操作[29]。不规则性胰腺切除术不规则的胰腺切除术包括保留十二指肠胰头切除术、胰腺中段切除术、胰腺肿瘤剜除术等,这些术式都有报道,且存在争议。对于治疗胰腺良性或低度恶性肿瘤时,在完整切除肿瘤的同时,最大程度保留了正常胰腺组织及周围正常脏器,广受医患认可,但又因其较高的并发症发生率和手术结果不确定性,使选择时左右为难。我院于2012年首次报道4例机器人辅助保留十二指肠胰头切除术,证明其是安全可行[30]。6年后又报道了回顾性研究,比较34例行机器人辅助保留十二指肠胰头切除术的病人与34例行机器人胰十二指肠切除术的病人,发现前者手术时间、术中估计出血量及外分泌功能不足的情况显著低于后者,但相对的并发症,尤其是胰漏发生率略高于后者[31]。Giulianotti等[32]于2004年至2005年首次完成3例机器人胰腺中段切除术,其中2例为浆液性囊腺瘤,1例为黏液性囊腺瘤,1例病人出现术后胰漏。之后在平均44个月的随访期间,未见病人内分泌或外分泌不足。我院于2016年报道有关机器人胰腺中段切除术的研究。该研究共纳入了100例病人,发现与开腹胰腺中段切除术相比,行机器人胰腺中段切除术的病人的住院时间、手术时间、估计术中出血量及临床术后胰漏率明显减少,术后恢复速度显著加快[33]。2017年,刘荣等[34]完成首例机器人胰腺中段切除、胰管成形合并胰腺端端吻合术,证明其可行性,但该术式的应用尚处于起步阶段,其远期疗效有待更长随访结果或随机临床试验以验证。2016年,Tian等[35]报道了一项针对<2 cm的胰腺神经内分泌肿瘤行机器人或传统胰腺肿瘤剜除术的回顾性研究,发现与开放手术相比,机器人手术没有增加术后胰漏或其他并发症发生率,并在手术时间及估计出血量方面有所减少。同年,我院[36]报道31例机器人胰腺肿瘤剜除术与25例传统胰腺肿瘤剜除术的回顾性研究结果,发现两种手术在手术时间(140 min比 100 min,P=0.009)、术中出血量(100 mL 比 30 mL,P=0.001)方面差异有统计学意义,而在术后并发症尤其是胰漏方面差异无统计学意义。其他机器人胰腺外科手术近年来,使用机器人辅助系统行联合血管切除的胰腺切除术越来越多。2011年,Giulianotti等[37]首次报道对局部进展期的胰腺肿瘤病人行联合血管切除及重建的机器人胰腺切除术,包括2例联合腹腔干及脾切除的胰体尾切除术,1例联合门静脉及脾切除的胰体尾切除术,2例联合门静脉切除的胰十二指肠切除术,术后1例病人因十二指肠溃疡再次入院手术,1例病人存在A级胰漏,1例病人存在腹腔积液,后均恢复良好。2018年,我院对开展的59例联合血管切除及重建的胰腺肿瘤根治术作了分析,其中机器人占20例,结果发现开腹或使用机器人辅助系统行该术式在手术时间、术后并发症发生率及再次手术率方面差异并无统计学意义[38]。2019年,Beane等[39]报道50例机器人联合血管切除及重建的胰腺切除术,进一步证实其安全性及可行性。此外,在其他胰腺外科手术方面,2009年,Giulianotti等[40]首次报道机器人胰体尾切除术合并自体胰岛移植,术后病人恢复可。2014年,Galvani等[41]报道了6例机器人全胰切除术合并自体胰岛移植,短期安全性可。2012年,Boggi等[42]报道3例机器人胰腺移植术,均未出现并发症。2015年,刘荣等[43]首次报道机器人辅助单孔腹腔镜胰腺切除术治疗胰尾部胰岛素瘤1例,术后病人恢复顺利,无并发症。2018年,Zureikat等[44]报道39例使用机器人平台对慢性胰腺炎病人行不同胰腺外科手术治疗的经验。可见,机器人平台可广泛应用于几乎所有胰腺手术。参考文献(略)
彭承宏 主任医师 上海瑞金医院 普外科4317人已读 - 精选 胰腺癌侵犯血管:挑战与争议
去年的一篇文章,原始出处:Sabater L, Muoz E, Roselló S, et al.Borderline resectable pancreatic cancer. Challenges and controversies. Cancer Treat Rev.2018 Jul;68:124-135.谈一下我的看法:胰腺癌预后很差,80%来了都没法手术,或局部进展侵犯大血管或转移播散,后者目前没有办法;前者通过影像学技术可筛选出一部分交界可切除患者,新辅助化疗又可以使其获得比较好的反应,这样的患者值得尝试手术。我对侵犯大血管的看法是:1.静脉侵犯不是问题;2.胰体尾癌腹腔干分叉处侵犯,胃十二指肠动脉好,可以行扩大的胰体尾癌切除;如胃十二指肠动脉也侵犯,由于胰体尾切除后,肝固有动脉与腹腔干距离变得极短,也可重建,需要详细评估;3.肠系膜上动脉侵犯,看侵犯范围,通常需要术中评估,根部侵犯较难获得根治,不一定推荐。总而言之:获得R0切除才有可能获益;必须在专业的胰腺中心施行上述手术,术后的管理是很大的挑战!
彭承宏 主任医师 上海瑞金医院 普外科6568人已读 - 精选 机器人手术开展的现状与展望
微创外科因为其良好的手术效果,例如痛苦小、恢复时间短、并发症发生率低,在过去二十年内得到了快速的发展,同时逐渐被广大患者广泛接受。微创技术给外科领域带来了革新,而机器人手术系统则进一步完善了微创手术的定义,开拓了新的视野。1987年,当Moret第一次报道完成了腹腔镜胆囊切除术时,就给外科手术带来了一场名为“微创”的革命。然而,在某些方面腹腔镜技术也有一定的局限性。如手术器械移动的限制(可自由活动度问题),二维的图像画面,图像的不稳定性(长时间持镜可能造成的频繁移动)以及对于外科医生来说不符合人体工程学的姿势及角度等。机器人手术系统为这些腔镜手术的缺陷提供了解决方法。历史早在80年代晚期,就已出现了一些简单的计算机辅助机器人手术系统,而其在腹部外科的应用与发展则开始于90年代初。1991年,Computer Motion公司首先为微创手术设计了世界第一个机器人装置。名为AESOP(automated endoscopic system for optimal positioning ),为一个声控的机器人手臂内镜摄像头。1993年,Cedars-Sinai医学中心的Jonathan Sackier医生实施了世界上首例机器人系统辅助腹腔镜胆囊切除术。2001年9月,J.Marescaux教授和他的团队第一个完成了远程外科手术(即Lindbergh手术)。目前,在不同程度的机器人辅助系统的帮助下,已完成了超过200000例外科操作,范围遍布几乎所有的外科领域。而机器人手术系统也已更加完善。机器人手术系统现在,常用的机器人系统包括Da Vinci系统和Zeus机器人。以Da Vinci系统为例,机器人系统包括三部分:操作台(图1)、机器人手臂(图2)及腔镜器械。操作台提供给医生的图像,来自于左右眼独立的取景器,系统通过模拟人脑的能力,整合图像偏差、产生视深度,从而给术者提供一个高清立体的三维图像。除了控制摄像头的机器人手臂外,Da Vinci系统还包括三个用来装配腔镜器械的机器人手臂。机器人系统的腔镜器械和开腹手术的人类手腕活动度一样,拥有7度的自由度(图3),而传统腔镜手术器械只有四度的活动自由度。外科医生可以坐在操作台前通过操纵类似于游戏手柄的操纵杆来控制机器人手臂完成精细的手术操作。机器人系统的优缺点机器人系统具有多项优点。首先,机器人系统能为术者提供高清的三维立体的图像画面,而不是仅依赖于偏光及颜色分离技术。因此,即使手术野由于镜头角度关系受到限制,但却有超乎想象的真实度。这套系统能使术者如同开腹手术一般看清周围的情况并同时具有放大缩小的功能。其次,机器人可以过滤掉外科医生在术中操作器械时的手部振颤。这种处理方式使外科手术达到了空前的精准性。再次,与传统腔镜相比,机器人的器械拥有接近人手的活动范围度以及能在极小的切口中超过360度的移动。最后,将机器人操作系统与远程通讯结合在一起就能完成远程协作手术。在过去的几十年里,机器人远程手术被用来消除距离的障碍。它可以使无法到达现场的医生参与并共同完成手术步骤。由于上述优势,机器人手术系统可以实现复杂手术的微创化。高昂的器械费用,是机器人系统的最大缺陷。一套Da Vinci系统约需数百万美金,而其每年的维护费用约为总价值的10%,此外还有手术器械的消耗费用。机器人系统的价格限制了它在大型医疗中心的作为手术首选的普及和对其技术的深入研究。它的其他缺点还包括缺乏触觉反馈等。机器人手术的现状与发展目前,机器人系统的应用几乎已涉及所有的外科领域。包括大部分的消化道手术(腔镜胆囊切除术,Nissen/Toupet胃底折叠术,肥胖症的胃转流手术,食管手术,直结肠、胰腺和肝脏手术)、泌尿外科手术(前列腺癌根治术、肾癌根治术)、妇科手术、机器人辅助胸腔镜等。虽然机器人系统弥补了很多传统腔镜上的不足,但就目前来说,它的普及还有很多的局限因素。首先,限制机器人系统普及的最主要的原因还是价格问题。我们相信,随着技术的发展,总会出现适应市场高需求的低成本机器人系统。此外,尽管机器人系统的三维图像系统能通过提高手术的安全性、精确度来弥补腔镜手术触觉反馈的缺乏。但是在一些病例中,缺乏触觉反馈仍会引起某些意外状况。因此,各种替代方案正在实施和研究当中。由于机器人系统的信息转换全由电子化控制,所以它使远程协作手术变成了可能。能够使发展中国家的患者在自己国家就能享受到世界知名外科医生的治疗。最后,通过虚拟现实技术与术前模拟的结合,机器人系统将会引领外科手术进入一个半自动甚至全自动远程手术的新时代。通过将病人解剖数据与三维重建的融合,可以使术者在术前对某个特定病人模拟的结果进行多次实践,从而找出对于该病人的最佳方案。结论在过去的近20年中,我们经历了从传统开腹手术到腹腔镜手术,从机器人手臂镜头辅助系统到机器人手术,最终到现在的远程协作手术。虽然目前机器人系统并没有普及到成为手术室的必备装备,但是如果能够预测未来的话,我们可以说,这只是一个时间问题。未来的机器人将会变得更小、更便宜、具有触觉反馈系统以及能够完成远程协作手术。目前,显而易见,机器人系统对于我们来说还是一项较先进的技术,其临床应用和优点仍有较大的发展空间。
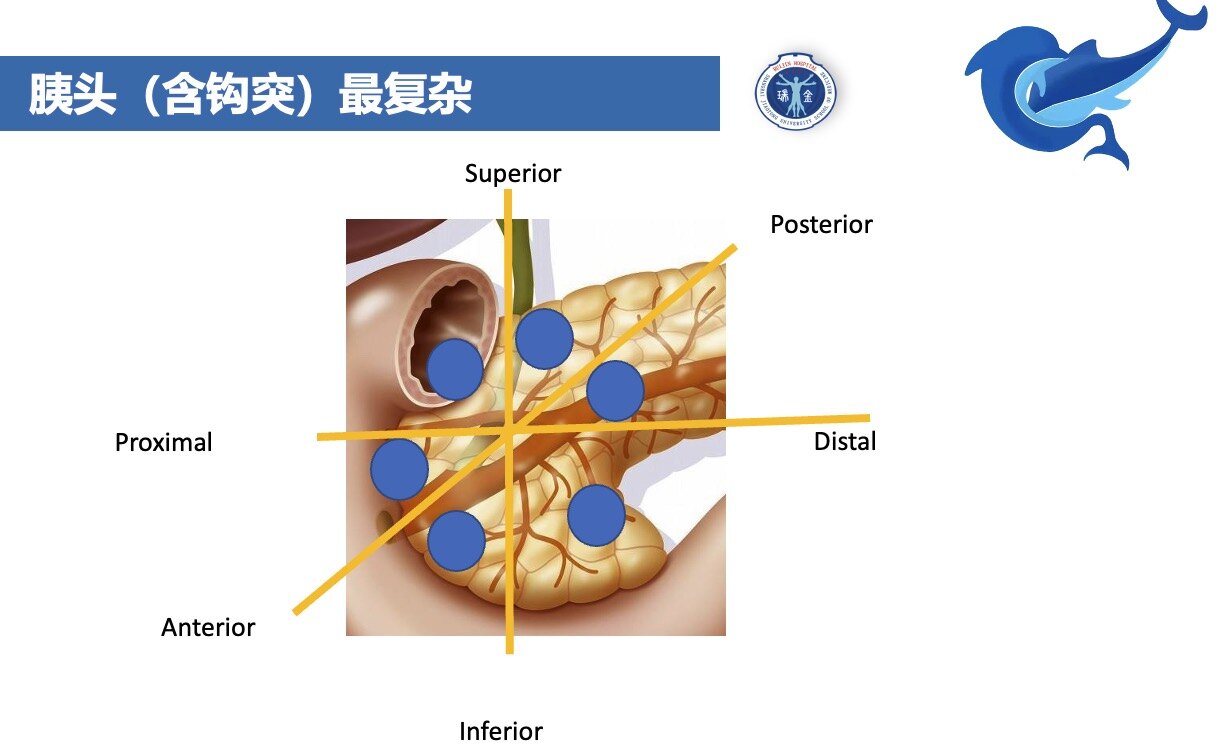
彭承宏 主任医师 上海瑞金医院 普外科3683人已读 - 机器人胰头肿瘤剜除,国际领先
今年,我们团队统计了瑞金医院胰腺外科2010-2021年机器人辅助胰头钩突肿瘤剜除术的短期及长期结果,证实了该技术治疗胰头钩突良性低度恶性肿瘤的可行性及临床获益,机器人组无1例C级胰瘘或VI/V级并发
 金佳斌 副主任医师 上海瑞金医院 普外科309人已读
金佳斌 副主任医师 上海瑞金医院 普外科309人已读 - IPMN恶变是否预后好于一般的胰腺导管腺癌?
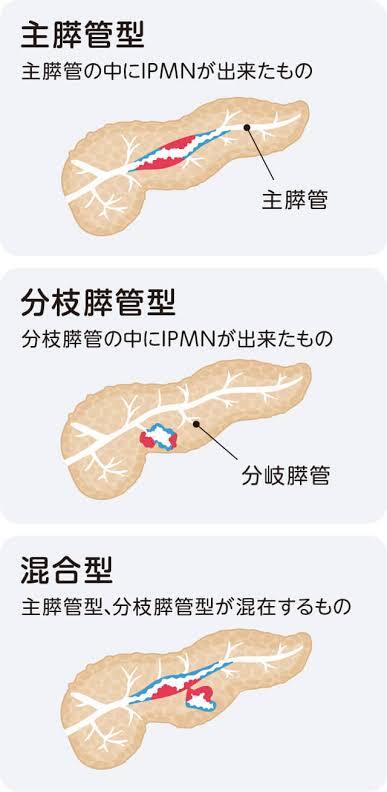
通常认为,IPMN一旦恶变,其等同于胰腺导管腺癌,处理原则也是一样的,但我们总有一种感觉,IPMN恶变后,一个是进展似乎没那么快,另一个就是手术效果更好,今天我们就来看一篇新鲜出炉的文章(2024年2月上线),总结了105例的恶变的IPMN,比较其和普通胰腺导管腺癌的肿瘤学特征。这是由梅奥诊所的Truty教授领衔的课题组所做的研究,Truty教授是位大牛,也是北美少数几位可以做胰腺癌联合动静脉切除重建的人,虽然没和他本人聊过,但感觉是属于人狠话不多那种😄课题组回顾了2011-2022年的胰腺癌切除术:胰腺导管腺癌1052例,其中65%接受术前新辅助化疗;恶性IPMN105例,其中25%接受术前新辅助化疗,结果发现,两组对术前新辅助化疗,病理反应无差异,PET,Ca199正常化,放射学改变也无差异。但是癌变后的IPMN在总生存率,无病生存率上有显著提高,进一步研究发现,恶性的IPMN切除后明显复发更少,相应的死亡也更少。通过生存率分析(中位随访时间25个月),研究团队发现,胰腺导管腺癌组5年总体生存率为29%,而IPMN恶变组为惊人的52%(p<0.001,具有显著差异,我也惊呆了🤯)。随访同样的,两组的无病生存时间也有显著差异(30%vs60%,p<0.001)。恶变的IPMN似乎患者年纪更大,更多的接受胰体尾切除和全胰腺切除,更少需要血管切除重建,更少接受术前新辅助化疗,术后的并发症也更少。这些似乎提示,IPMN恶变往往发展较慢(和我前文提到的呼应),全胰腺切除更是应对这个疾病本身的特色,也就是主胰管型的IPMN往往是整个胰腺的病变,此时全胰腺切除更适合治本。也是这一点导致了做胰十二指肠切除的患者反而少,那么并发症,尤其是胰肠吻合口瘘自然就不存在。另外,由于很大一部分恶变的IPMN术前不为人知,或不确定是否恶变而选择直接手术,所以新辅助化疗的比例更低。最后研究人员分析发现IPMN恶变切除术后6个月内复发更低,多因素分析提示IPMN恶变是胰腺癌术后低复发和死亡的独立预测因素,从而告诉我们,这些所谓的“胰腺癌“预后更好。尽管100多例的恶变IPMN样本量仍不够多,但已经是目前最大宗的样本量研究了,给了我们很好的提示,我们临床一直以来有的感觉,是真实的,IPMN恶变,应该积极的去切除,在术前诊断考虑有淋巴结转移或血管侵犯的情况下,也该做术前新辅助化疗,预后更好。Fogliati,A.,Zironda,A.,Fiorentini,G.etal.OutcomesofNeoadjuvantChemotherapyforInvasiveIntraductalPapillaryMucinousNeoplasmComparedwithdeNovoPancreaticAdenocarcinoma.AnnSurgOncol(2024).https://doi.org/10.1245/s10434-023-14875-5
 金佳斌 副主任医师 上海瑞金医院 普外科1123人已读
金佳斌 副主任医师 上海瑞金医院 普外科1123人已读





